دراسة تحدد عقار "إيفوشيلد" بفعّالة التحييد ضد متحوّر "أوميكرون"
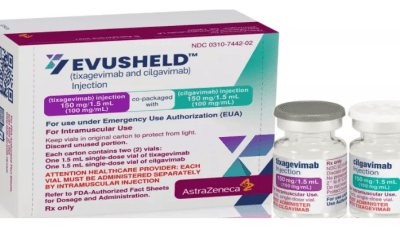
أكدت البيانات الأولية الناتجة عن دراسة مستقلة أجرتها إدارة الغذاء والدواء الأمريكية على احتفاظ عقار "إيفوشيلد" المضاد لكوفيد-19، تركيبة الأجسام المضادة طويلة المفعول tixagevimab)/ cilgavimab) من "أسترازينيكا"، بفعالية التحييد ضد متحور "أوميكرون" (B.1.1.529) من فيروس "سارس-كوف-2".
واستخدمت الدراسة مقياس "التركيز المثبط 50" لتحديد قدرة التحييد التي يتمتع بها الجسم المضاد، حيث سجّل عقار "إيفوشيلد" معدلاً قدره 171 نانوغرام بالمليلتر ومعدل 277 نانوغرام بالمليلتر في اختبارين تأكيديين، وتقع هذه الأرقام ضمن نطاق التحييد المعياري الذي يمكن رصده عند المصابين سابقاً بمرض كوفيد-19. وعلى صعيد السلالة الأصلية لفيروس "سارس-كوف-2" والمعروفة سابقاً باسم "سلالة ووهان"، سجل "إيفوشيلد معدل "تركيز مثبط" يقارب 1.3 نانوغرام بالمليلتر و1.5 نانوغرام بالمليلتر في اختبارين متتاليين.
وتأتي البيانات المبكرة الناتجة عن اختبار الفيروس الزائف لاستجابة بروتين "سبايك" الكامل في متحور "أوميكرون" لتركيبة الأجسام المضادة tixagevimab)/ cilgavimab) في "إيفوشيلد"، لتعزز المجموعة المتنامية من الأدلة قبل السريرية التي تؤكد على احتفاظ "إيفوشيلد" بنشاط التحييد ضد جميع المتحورات المثيرة للقلق التي تم اختبارها حتى تاريخه.
وقام بإجراء الدراسة عدد من المحققين المستقلين في "مركز التقييم والأبحاث البيولوجية" في إدارة الغذاء والدواء الأمريكية، بدعمٍ من التمويلات البحثية التي تقدمها الحكومة الأمريكية.
وفي هذا السياق، قال ميني بانغالوس، نائب الرئيس التنفيذي لشؤون أبحاث وتطوير المستحضرات الدوائية الحيوية لدى "أسترازينيكا": "أكدت الدراسة احتفاظ عقار ’إيفوشيلد‘ بفعالية التحييد ضد متحور ’إوميكرون‘. فمن خلال الجمع بين اثنين من الأجسام المضادة القوية اللذان يتميزان بنشاطين مختلفين يكملان بعضهما البعض، تم تصميم ’إيفوشيلد‘ للتغلب على المقاومة التي قد تظهرها المتحورات الجديدة من فيروس ’سارس-كوف-2‘. ويعد ’إيفوشيلد‘ تركيبة الأجسام المضادة طويلة المفعول الوحيدة التي تحصل على ترخيص الاستخدام الطارئ في الولايات المتحدة لأغراض الوقاية قبل التعرض لكوفيد-19، إضافة إلى التراخيص التي حصل عليها في عدّة بلدان أخرى، ونعمل أيضاً إلى جانب الجهات التنظيمية المعنية فيما يخص طلبات ترخيص استخدام ’إيفوشيلد‘ لعلاج كوفيد-19".
ونظراً لأن التجارب السريرية لعقار "إيفوشيلد" انطلقت قبل انتشار متحور "أوميكرون"، تعمل الشركة على جمع المزيد من البيانات لتحقيق فهمٍ أفضل للتأثيرات على الممارسات السريرية. وفي الوقت الراهن، تجري "أسترازينيكا" وعدد من المختبرات الخارجية تحليلات إضافية لتقييم فعالية "إيفوشيلد" ضد متحور "أوميكرون"، ومن المتوقع توفر البيانات في القريب العاجل.
وفي شهر ديسمبر 2021، حصل عقار "إيفوشيلد" على ترخيص الاستخدام الطارئ من إدارة الغذاء والدواء الأمريكية لأغراض الوقاية قبل التعرض لكوفيد-19، لمن يعانون ضعفاً متوسطاً إلى شديد في المناعة نتيجة حالات صحية معينة أو تناول الأدوية المثبطة للمناعة، والذين قد تعجز أجسامهم عن تحقيق استجابة مناعية كافية للقاح المضاد لكوفيد-19، إضافة إلى الذين لا يوصى بإعطائهم اللقاح المضاد لكوفيد-19. ومن المتوقع توفر الجرعات الأولى في غضون أيام.
ويعاني حوالي 2% من سكان العالم من المخاطر المتزايدة التي يفرضها عجز الجسم عن توليد استجابة مناعية كافية للتطعيم بلقاح كوفيد-19. وتشير الأدلة الصاعدة إلى أهمية حماية الفئات السكانية المعرضة للخطر من الإصابة بكوفيد-19 لمنع تطور الفيروس، ويعد هذا عاملاً مهماً وراء ظهور المتحورات.
ووفقاً لبيانات المرحلة الثالثة من تجربة TACKLE للمرضى الذين يتلقون علاجهم خارج المستشفيات، أظهر عقار "إيفوشيلد" قدرته على تقليل خطر تطور الإصابة بكوفيد-19 إلى مراحل خطرة أو الوفاة (لأي سبب) بنسبة 50%، مقارنة بالمرضى الذين لم يدخلوا المستشفيات وتلقوا جرعات وهمية وكانوا يعانون من أعراض خفيفة إلى متوسطة من كوفيد-19 لمدة سبعة أيام أو أقل.
-انتهى-
حول عقار "إيفوشيلد":
يعتبر عقار "إيفوشيلد"، المعروف سابقاً باسم AZD7442، تركيبة تضم اثنين من الأجسام المضادة طويلة المفعول – tixagevimab (AZD8895) و cilgavimab (AZD1061) – المشتقة من الخلايا البائية التي تبرع بها المرضى الذين تماثلوا للشفاء بعد إصابتهم بفيروس "سارس-كوف-2". وترتبط هذه الأجسام المضادة البشرية وحيدة النسيلة، التي اكتشفها الباحثون في المركز الطبي لجامعة فاندربيلت وحصلت "أسترازينيكا" على رخصة استخدامها خلال شهر يونيو 2020، بمواقع مميزة على سطح البروتين التاجي "سارس-كوف-2"8،1 وتم تحسينها بواسطة "أسترازينيكا" من خلال تمديد عمر النصف للأجسام المضادة وحجب الارتباط بمستقبلات منطقة الشدفة المتبلورة (Fc receptor) والارتباط بالبروتين المتمم C1q. ويسهم تمديد عمر النصف بمضاعفة فعالية تأثير الأجسام المضادة بواقع أكثر من ثلاثة أضعاف بالمقارنة مع الأجسام المضادة التقليدية، لتتمكن بذلك من توفير ما يصل إلى 12 شهراً من الحماية ضد مرض كوفيد-19 بعد جرعة واحدة؛14،12 وتظهر البيانات المستمدة من نتائج التجارب السريرية للمرحلة الثالثة من دراسة PROVENT قدرة العقار على توفير حماية تدوم لمدة ستة أشهر على الأقل15. بينما يهدف حجب الارتباط بمستقبلات منطقة الشدفة المتبلورة (Fc receptor) لتقليص مخاطر التعزيز المعتمد على الجسم المضاد – وهي ظاهرة تشهد تسبب الأجسام المضادة الخاصة بالفيروس بتعزيز العدوى و/ أو المرض بدلاً من تثبيطها16.
وفي شهر ديسمبر 2021، حصل عقار "إيفوشيلد" (tixagevimab)/ cilgavimab) على ترخيص الاستخدام الطارئ من إدارة الغذاء والدواء الأمريكية لأغراض الوقاية قبل التعرض لفيروس كوفيد-19، وهو التركيبة الوحيدة المرخصة في الولايات المتحدة للوقاية من أعراض كوفيد-19 قبل التعرض للفيروس، كما أنه حاصل على ترخيص الاستخدام الطارئ للوقاية من كوفيد-19 في عدة بلدان أخرى.
وفي شهر أغسطس 2021، أعلنت "أسترازينيكا" أن عقار "إيفوشيلد" أظهر انخفاضاً ذو دلالة إحصائية في مخاطر الإصابة بأعراض كوفيد-19 في دراسة PROVENT؛ حيث سجل العقار فعالية تقدر بنسبة 83% بالمقارنة مع العلاج الوهمي (البلاسيبو) في الدراسة التحليلية التي استمرت على مدى سنة أشهر وأُعلن عن نتائجها في 18 نوفمبر 2021. وفي شهر أكتوبر 2021، أعلنت "أسترازينيكا" عن تسجيلها لنتائج إيجابية عالية المستوى في التجارب السريرية للمرحلة الثالثة من دراسة العلاج في العيادات الخارجية TACKLE لعقار "إيفوشيلد". وعلاوة على ذلك، تجري دراسة فعالية عقار "إيفوشيلد" كعلاج محتمل لمرضى كوفيد-19 المدخلين إلى المستشفيات تحت إطار تجربة ACTIV-3 التي تجريها المعاهد الوطنية للصحة، وفي تجربة علاجية تعاونية أخرى تركز على المرضى المدخلين إلى المستشفيات.
ويجري تطوير "إيفوشيلد" بدعمٍ من الحكومة الأمريكية، ويشمل ذلك تمويلات اتحادية من وزارة الصحة والخدمات الإنسانية؛ مكتب السكرتير المساعد للاستعداد والاستجابة؛ هيئة التطوير والأبحاث الحيوية الطبية المتقدمة بالشراكة مع وزارة الدفاع؛ المكتب التنفيذي للبرنامج المشترك للدفاع الكيميائي والبيولوجي والإشعاعي والنووي بموجب العقد رقم (W911QY-21-9-0001).
وبموجب شروط اتفاقية الترخيص المبرمة مع جامعة فاندرفيلت، ستدفع "أسترازينيكا" رسوم امتياز من خانة واحدة على صافي المبيعات المستقبلية.
وتعد "أسترازينيكا" (المدرجة في سوق لندن للأوراق المالية وبورصة ستوكهولم وناسداك بالرمز AZN) شركة عالمية رائدة في مجال المستحضرات الدوائية الحيوية، تستند في عملها إلى أحدث العلوم وتركز على استكشاف وتطوير والطرح التجاري للأدوية القائمة على الوصفات الطبية في مجالات علم الأورام والمستحضرات الدوائية لأمراض القلب والشرايين والكلى والاستقلاب والجهاز التنفسي والمناعة. تتخذ "أسترازينيكا" من كامبريدج بالمملكة المتحدة مقراً لها، وتزاول نشاطها في أكثر من 100 دولة، ويستفيد من علاجاتها المبتكرة أكثر من مليون مريض حول العالم. ولمزيد من المعلومات، يرجى زيارة الموقع الإلكتروني: astrazeneca.com ومتابعة حساب الشركة على "تويتر": @AstraZeneca.
المراجع:
ACTIV. National Center for Advancing Translational Sciences OpenData Portal. SARS-CoV-2 Variants & Therapeutics, All Variants Reported in vitro Therapeutic Activity. Available at: https://opendata.ncats.nih.gov/variant/activity [Last accessed: December 2021].
Neerukonda, S.N. et al. Establishment of a well-characterized SARS-CoV-2 lentiviral pseudovirus neutralization assay using 293T cells with stable expression of ACE2 and TMPRSS2. PLOS ONE March 10, 2021. Available at https://journals.plos.org/plosone/article?id=10.1371/journal.pone.0248348 [Last accessed December 2021].
Oliver, S. Data and clinical considerations for additional doses in immunocompromised people. ACIP Meeting July 22, 2021. Available at: https://www.cdc.gov/vaccines/acip/meetings/downloads/slides-2021-07/07-COVID-Oliver-508.pdf. [Last accessed: December 2021].
AstraZeneca data on file.
Corey L, et al. SARS-CoV-2 Variants in Patients with Immunosuppression. N Engl J Med. 2021; 385:562-566. DOI: 10.1056/NEJMsb2104756.
AstraZeneca news release. Evusheld reduced risk of developing severe COVID-19 or death in TACKLE Phase III outpatient treatment trial. Available at: https://www.astrazeneca.com/content/astraz/media-centre/press-releases/2021/Evusheld-phiii-trial-positive-in-covid-outpatients.html. [Last accessed: December 2021].
Dong J, et al. Genetic and structural basis for recognition of SARS-CoV-2 spike protein by a two-antibody cocktail. bioRxiv. 2021; doi: 10.1101/2021.01.27.428529.
Robbie GJ, et al. A novel investigational Fc-modified humanized monoclonal antibody, motavizumab-YTE, has an extended half-life in healthy adults. Antimicrob Agents Chemother. 2013; 57 (12): 6147-53.
Griffin MP, et al. Safety, tolerability, and pharmacokinetics of MEDI8897, the respiratory syncytial virus prefusion F-targeting monoclonal antibody with an extended half-life, in healthy adults. Antimicrob Agents Chemother. 2017; 61(3): e01714-16.
Domachowske JB, et al. Safety, tolerability and pharmacokinetics of MEDI8897, an extended half-life single-dose respiratory syncytial virus prefusion F-targeting monoclonal antibody administered as a single dose to healthy preterm infants. Pediatr Infect Dis J. 2018; 37(9): 886-892.
AstraZeneca news release. New analyses of two AZD7442 COVID-19 trials in high-risk populations confirm robust efficacy and long-term prevention. Available at: https://www.astrazeneca.com/media-centre/press-releases/2021/new-analyses-of-two-azd7442-covid-19-phase-iii-trials-in-high-risk-populations-confirm-robust-efficacy-and-long-term-prevention.html. [Last accessed: December 2021].
van Erp EA, et al. Fc-mediated antibody effector functions during respiratory syncytial virus infection and disease. Front Immunol. 2019; 10: 548.